记忆力减退通常是阿尔茨海默氏病的第一个征兆,其次是混乱和思维困难。这些症状反映了脑组织损伤恶化的典型模式。有毒的蛋白质簇首先集中在大脑的颞叶——记忆区——然后扩散到大脑中对思考和计划很重要的部分。
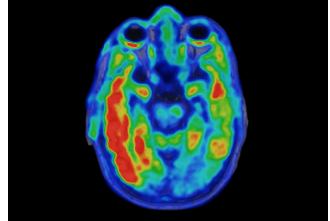
位于圣路易斯的华盛顿大学医学院的研究人员进行的一项研究提供了一些线索,说明为什么大脑的某些部位特别容易受到阿尔茨海默氏症的损害。它归结为 APOE 基因,这是阿尔茨海默病的最大遗传风险因素。他们发现,大脑中 APOE 最活跃的部分是受到伤害最大的区域。
该研究结果于 11 月 16 日发表在《科学转化医学》杂志上,有助于解释为什么阿尔茨海默氏病的症状有时会有所不同,并强调了阿尔茨海默氏病未被充分研究的方面,这表明尚未发现的生物学机制可能在该疾病中发挥重要作用。
“有一些罕见的、非典型的阿尔茨海默氏症,其中人们首先出现语言或视觉问题,而不是记忆问题,”资深作者 、医学院 Mallinckrodt 放射学研究所放射学助理教授Brian A. Gordon 博士说. “当你扫描他们的大脑时,你会看到语言或视觉区域的损伤,而不是记忆区域。患有非典型阿尔茨海默氏症的人经常被排除在研究之外,因为研究一个每个人都有相同症状的群体更容易。但这种异质性告诉我们,关于阿尔茨海默氏症如何以及为何以这种方式发展,我们仍然有一些事情不了解。某些大脑区域受损而不是其他区域是有原因的,我们还不知道那个原因。我们发现的关于这种疾病的每一个谜团都使我们更接近我们需要解决的问题。”
阿尔茨海默病始于一种称为淀粉样蛋白的脑蛋白。在人们出现神经系统问题的最初迹象之前的二十年或更长时间,这种蛋白质就开始形成斑块。经过多年的淀粉样蛋白积累,tau 蛋白(另一种脑蛋白)开始形成缠结。不久之后,受影响区域的组织开始枯萎和死亡,认知能力开始下降。
为了解阿尔茨海默病脑损伤发生的原因,戈登及其同事——包括第一作者、戈登实验室的技术员艾琳·丁瑟——研究了 350 名志愿参加记忆和衰老研究的人,这些人通过医学院的查尔斯·F. 和乔安妮· 奈特阿尔茨海默病研究研究中心。参与者接受了脑部扫描,因此研究人员可以测量淀粉样斑块和 tau 蛋白缠结的数量和位置,以及各个脑区的体积。
研究人员将志愿者的蛋白质团块和组织损伤模式与 APOE 和其他与阿尔茨海默病相关基因的基因表达模式进行了比较,如艾伦人类大脑图谱中所描绘的那样,这是一份由人类大脑中的基因表达详细图谱编制的艾伦脑科学研究所。
“你看到 APOE高表达的地方与你看到 tau 缠结和组织损伤的地方非常匹配,”戈登说,他也是心理和脑科学助理教授。“而且不仅仅是 APOE。例如,如果您查看与阿尔茨海默病相关的前 20 个基因,它们都以相似的模式在颞叶中表达。这些区域有一些根本不同的东西,使它们容易受到阿尔茨海默氏症的脑损伤,这种差异可能是从出生开始就存在的,并受到一个人遗传学的影响。”
每个人都携带某种版本的 APOE 基因,但携带 APOE4 变体的人患阿尔茨海默病的可能性是普通人群的 12 倍,而且年龄更小。阿尔茨海默病研究人员早就知道 APOE4 会增加人们大脑中淀粉样蛋白的积累。David Holtzman 医学博士、Barbara Burton 和 Reuben M. Morriss III 神经病学特聘教授及其同事研究了tau 蛋白缠结而非淀粉样蛋白斑块的小鼠, 结果表明 APOE4 也会增加 tau 蛋白引起的损伤,即使没有淀粉样蛋白存在。
为了评估APOE的高风险变异对 人类 tau 相关脑损伤的影响,研究人员将每个参与者分类为是否携带高风险变异,并分析了他们大脑中的蛋白质簇和萎缩。
“ APOE4 携带者更有可能开始积累淀粉样蛋白,这使他们走上了阿尔茨海默氏症的道路,”戈登说。“然后,对于相同数量的淀粉样蛋白,它们会产生更多的 tau 蛋白缠结,从而导致更多的萎缩。这是对大脑的双重打击。”
在未来的工作中,Gordon 及其同事计划探索基因表达模式如何与非典型阿尔茨海默氏症患者的 tau 损伤模式相关。
“当我们看到有视力问题的人时,是否存在与大脑受损区域相对应的特定遗传特征?” 戈登问道。“我们想知道为什么有些人会出现这些改变的模式,以及这对阿尔茨海默病的发展方式和治疗方式意味着什么。”
标签:
免责声明:本文由用户上传,如有侵权请联系删除!
